Хлорид меди – это соль, которая нашла широкое применение в промышленности. Её используют в металлургии для защиты металлов от коррозии, применяют в фармацевтике для изготовления лекарственных препаратов. Хлориды меди востребованы в химии и на предприятиях по переработки нефти. Вещество крайне токсично, при работе с ним требуется соблюдать меры безопасности.
Содержание
Что такое хлорид меди, виды, формулы
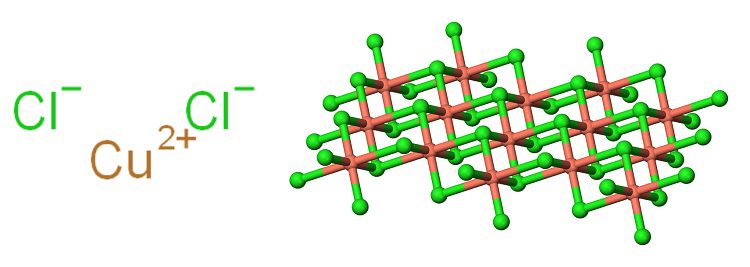
Хлорид меди – это соединение, относящееся к классу солей. Состоит из амфотерного металл меди и остатка соляной кислоты. Поскольку медь имеет несколько валентностей (1 и 2), она образует хлориды разных типов. Формула хлорида меди I – CuCl, хлорида меди II – CuCl2.
Хлорид меди II находят в природе в виде минерала – эрнохальцита. Это редкое образование в виде мелких пластинчатых кристаллов синего цвета. Хлорид меди I выделил англо-ирландский натуралист – Роберт Бойль. Он сделал своё открытие в 1666 году путём добавления металлической меди к хлористой ртути. Однако как вещество хлорид меди I было описано лишь спустя более 100 лет. Свойства раствора хлорида подробно задокументировал французский химик Жозеф Луи Пруст.
Физические свойства, внешний вид
При нормальных условиях хлорид меди I – мелкодисперсный порошок, состоящий из зеленоватых кристалликов, плотность 4,145 г/см3. При подогревании цвет изменяется на синий. Термоустойчив, плавится при 426 °С, закипает при повышении температурного режима до 1490 °С, не разлагается под действием высоких температур. Хлорид меди I плохо растворяется в воде, но лучше в органических растворителях: спиртах, феноле, толуоле, эфирах. Распространён раствор хлорида меди в кислоте. Возможно растворение хлорида меди в растворе аммиака.
Хлорид меди II — это порошкообразные голубовато-зеленоватые кристаллы с высокой гигроскопичностью. Легко впитывает воду и при её выпаривании образует кристаллогидраты. Их структура и атомарный состав зависит от температуры образования:
- при 117 °С – CuCl2 ∙ H2O;
- при невысоком нагреве (менее 42 °С) – CuCl2 ∙ 2H2O;
- при разогревании до 26 °С и ниже образуется CuCl2 ∙ 3H2O;
- менее 15 °С – CuCl2 ∙ 4H2O.
Легко образуется раствор хлорида меди II с этанолом, водой, метанолом, а также ацетоном. Способен быстро менять степень окисления до +1 и 0.
Химические свойства, реакции
Хлорид меди I вступает в специфическую реакцию – дисмутацию. В ходе данного взаимодействия медь функционирует и как окислитель, и как восстановитель. При этом в продуктах реакции она находится с разным условным зарядом. Пример такой реакции – кипячение при 100 °С:
CuCl → CuCl2 + Cu↓
При погружении хлорида меди в хлороводород происходит необратимое расщепление с образованием комплекса:
СuCl + HCl → H[CuCl2]
На влажном воздухе хлорид меди постепенно окисляется. Такая реакция приводит к выделению гидроксид-хлорида меди:
4CuCl + O2 + 2H2O → 4CuCl(OH)
Реакция хлорида меди с азотной кислотой даёт нитрат и бурый газ:
CuCl + 3HNO3 → Cu(NO3)2 + HCl + NO2↑ + H2O
Раствор хлорида меди вступает в реакцию с ацетиленом и аммиаком:
CuCl + C2H2 + NH3 → Cu2C2↓ + 2NH4Cl
Из уравнения хлорида меди II видно, что он более реактивно активен. Реагирует со щёлочью: реакция с едким натром преобразует исходное соединение в хлорид натрия:
CuCl2 + 2NaOH → 2NaCl + Cu(OH)2↓
Для хлорида меди характерна окислительно-восстановительная реакция с иодидом:
2CuCl2 + 4NaI → 2CuI + I2↑ + 4NaCl
При пропускании через раствор электрического тока запускается реакция электролиза:
CuCl2 → Сu↓ + Cl2↑
Хлорид меди осаждает сероводород. Эта реакция протекает с выделением черного осадка:
CuCl2 + H2S → CuS↓ + 2HCl
Производство и получение
В лабораториях хлорид меди 1 получают путём восстановления хлорида меди 2 при 80 °С:
CuCl2 + Cu → 2СuCl
Реактивом может выступать и медный купорос. Взаимодействие отражено в уравнении хлорида меди:
2CuSO4 + 2NaCl + SO2 + 2H2O → 2CuCl↓ + 2H2SO4 + Na2SO4
В промышленности получают за счёт реакции термолиза, уравнение хлорида меди:
2CuCl2 → 2CuCl + Cl2↑
Прямой синтез хлорида меди II:
Cu + Cl → CuCl2
Его получают и посредством обработки оксида:
CuO + 2HCl → CuCl2 + H2O
Крупные производители для выпуска хлорида меди применяют хлорирование в двух вариантах:
- CuS + Cl2 → CuCl2 + S↓
- CuS + 2NaCl + 2O2 → CuCl2 + Na2SO4
Применение
Как вещество хлорид меди распространён во всех областях. Наиболее востребовано применение в качестве реактива в органике и неорганике, а также крекинге, создании металлических и пиротехнических изделий, текстиля, целлюлозы. Хлориды меди необходимы для газового анализа и добычи меди.
Применение в нефтехимии и химпроме
Хлорид меди применяют для меднения поверхностей для защиты их от коррозии. Коррозийные поражения ухудшают внешний вид и функционал автомеханизмов, приводят к разрушению наиболее важных деталей. Тонкая плёнка меди на алюминиевой посуде и частях автотранспорта не позволяет кислороду воздуха связываться с железом и нарушать его структурную целостность.
При очистке нефтепродуктов хлорид меди выступает катализатором для реакций крекинга – разложение нефти на фракции в специализированных установках. Он ускоряет процесс крекированы, не связываясь с продуктами переработки.
Применение хлорида меди для получения красителей оправдано его стабильностью и богатой зеленовато-синей цветовой гаммой. Он незаменим для титриметрического анализа, широко используемого в аналитике, для нормального прохождения реакции декарбоксилирования – отделение диоксида углерода от карбоксильной группировки.
Применение в медицине, текстильной промышленности
При окрашивании тканей хлорид меди — это протрава, которая позволяет качественно зафиксировать окрас, придать ему большую яркость и насыщенность, избежать выцветания.
Раствор хлорида меди – действующее вещество растворов для парентерального введения. Применение основано на способности хлорида меди восполнять дефицит микроэлемента, необходимого для построения соединительных тканей организма (костей, хрящей), нормального функционирования нервной системы.
Инструкция по применению
Показания
Инструкция по применению гласит, что хлорид меди в комплексе с другими солями назначается как добавка к основному рациону при питании пациента с помощью внутривенной инфузии при обширных хирургических вмешательствах, химиотерапии, некрозах и энтеритах.
Противопоказания
Главное противопоказание – индивидуальная непереносимость компонентов. Она выражается в острой аллергической реакции. Производитель указывает в инструкции по применению, что средство не рекомендуется вводить детям до 10 лет, при печёночной недостаточности и непроходимости желчных протоков.
Способ применения и дозы
10 мл препарата добавляют в раствор аминокислот и белков, добиваясь доли в 50%. Суточная доза для взрослых больных с массой тела более 40 кг – 10 мл. Для людей, которые весят 14-40 кг дозу рассчитывают исходя из соотношения: 0,1 мл/кг в день.
Побочные действия
В инструкции по применению описаны наиболее вероятные побочные эффекты:
- тошнота и рвота;
- аллергия;
- тромбоз с воспалением стенки вены.
Беременность, лактация
Средство не рекомендуется применять беременным и кормящим женщинам.
Где купить и сколько стоит
Хлорид меди оптом продают заводы-производители. Стоимость 1 кг от 150 рублей. Более мелкие партии продаются в магазинах лабораторных реактивов по цене от 750 рублей за 100 грамм. Препараты с хлоридом меди продаются в аптеках, средняя стоимость 2150 рублей.
Заключение
Хлорид меди – это вещество, в зависимости от типа быстро поглощает воду либо не растворяется в ней. Оба варианта широко используются в различных сферах. Хлорид меди — это катализатор и реактив для реакций разделения нефтепродуктов, производства красящих составов. Он играет роль протравы, защищает от ржавчины, применяется для выпуска растворов для поддерживающей терапии больных, которые не могут питаться нормальным способом.
Читайте также:















Оставить комментарий