Карбонат аммония – это вещество, которое бывает техническим и пищевым. Технический карбонат аммония категорически запрещено употреблять в пищу! Концентрат легко провоцирует отравление с летальным исходом. Рассмотрим, что такое углеаммонийная соль, чем отличается пищевая от технической, формулы, уравнения, влияние на человеческий организм, применение вещества и другую информацию.
Содержание
Что такое карбонат аммония
Карбонат аммония – это прозрачная синтезированная гранулообразная субстанция лабораторного происхождения (нашатырно-спиртовой раствор). Производное углекислоты и солей аммония. Также существует в виде серых, белых или розоватых кристаллов с выраженным аммиачным ароматом. В пищевой промышленности вещество зарегистрировано, как пищевая добавка Е503.
Дополнительные наименования:
- углекислый аммоний;
- углеаммонийные соли;
- бикарбонат аммония.
Физические и химические свойства карбоната аммония, реакции
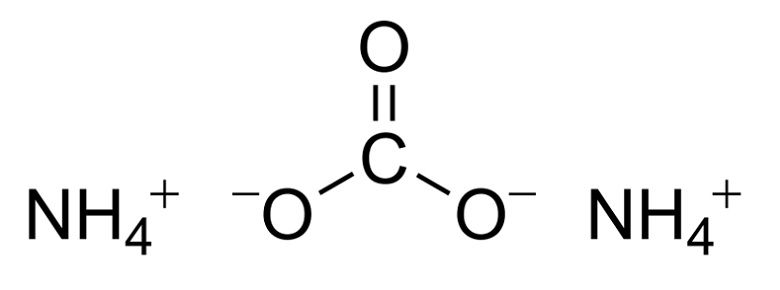
Формула: (NH4)2CO3
Высокая растворимость в Н₂О. Контактируя с кислородом, при температуре до 18-24ºС проявляет неустойчивость, превращаясь в аммониевый гидрокарбонат, выделяя аммиак. При 60ºС разлагается на аммиак, Н₂О и углеродный оксид.
Физические свойства
Свойства карбоната аммония:
- Плотность: 1,6 г/см³;
- Терморазложение: 60°C;
- Масса: 96 г/моль;
- Растворимость в Н₂О: (0°C); 100,1 (15°C); Разл. (100 °C).
Уравнение гидролиза:
(NH4)2CO3 + H2O ↔ NH4HCO3 + NH3 * H2O
Молекулярная реакция:
(NH4)2CO3+ HOH ↔ NH4CO3 + NH4OH (молекулярное уравнение)
Химические свойства, реакции с карбонатом аммония
Аммониевый карбонат при взаимодействии с водой разлагается, как слабокислая соль и слабые электролиты:
(NH₄)₂CO₃+ HOH ↔ NH₄CO₃ + NH₃OH
Ионная диссоциация:
NH₄⁺ + HOH↔NH₄OH + H⁺
Ионная реакция:
2NH₄⁺ + CO₃²⁻ + HOH ↔ HCO₃- + NH₄OH
Анионный гидролиз:
CO₃²⁻ + HOH ↔ HCO₃⁻ + OH⁻
Катионный:
NH₄⁺ + HOH↔NH₄OH + H⁺
Терморазложение:
(NH₄)₂CO₃ → CO₂↑ + 2NH₃↑ + H₂O↑
Взаимодействует с кислотами, поскольку СО₂ слабейшая из синтетических окислителей:
(NH₄)₂CO₃+ H₂SO₄ → (NH₄)₂CO₄ + CO₂↑ + H₂O
Реакция с диссоциирующими электролитами:
(NH₄)₂CO₃ + NaOH → Na₂CO₃ + 2NH₃↑ + 2H₂O
Реагирует с солями:
(NH₄)₂CO₃ +СaCl₂ → CaCO₃↓ + 2NH₄Cl
Взаимодействие с кислотами:
(NH4)2CO3+ H2SO4 = (NH4)2SO4 + CO2↑ + H2O.
С щелочной средой:
(NH4)2CO3+ NaOH = Na2CO3 + 2NH3↑ + 2H2O.
Получение и производство карбоната аммония
До появления современных технологий пищевую добавку Е503 извлекали из костных тканей, рогов, ногтевых пластин и др. азотных веществ, путем высокотемпературной перегонки жидкости. Сейчас добывают только в лабораторных условиях:
- Смешивая водяной пар, углекислоту и газообразный аммиак.
- При распаде аммония хлористого.
- Обработке жидкого аммиака углеродной двуокисью.
Раствор карбоната аммония добывают, путем насыщения углекислотой или реакцией между водой, аммиаком, углекислотой. Зачастую используют оба метода. 1-й, чтобы получить жидкую форму, затем выводят углеродную двуокись и аммиак для твердой.
Пищевая добавка Е503
Пищевая добавка Е503 – это смесь продуктов распада карбоната аммония. Не концентрированная субстанция. Пищевая добавка Е503 не распадается при комнатном давлении и температуре, чем и отличается от технического вещества.
Сферы применения карбоната аммония
Различные формы (твердая, жидкая) карбоната аммония, позволяют использовать вещество в различных индустриях.
Применение карбоната аммония в пищевой промышленности
Карбонат аммония незаменим при изготовлении кондитерских и хлебобулочных изделий, например бубликов, тортов. Применяют, в качестве дрожжей или соды для активации брожения и поднятия пышного теста. В оригинальных Скандинавских изделиях, используется исключительно пищевая добавка Е503. Применение традиционных дрожжей изменяет вкус готового печенья.
Также в пекарнях используют углекислый аммоний, в качестве разрыхлителя. Выделяя углекислоту, оказывает разрыхляющее действие. При изготовлении какао напитков, стабилизирует вкус и цвет.
Применение карбоната аммония в фармацевтике
В медицине карбонат аммония полезен для приготовления лекарственных средств, например, противокашлевых сиропов и местнораздражающих веществ для возбуждения чувствительных нервных окончаний верхних дыхательных путей – нашатырный спирт.
Применение карбоната аммония в виноделии
Пищевую добавку Е503 используют для винных напитков. Элемент ускоряет брожение, превращая сахар в алкоголь.
Применение карбоната аммония в восметологии
Карбонат аммония применяют для оттеночной стабилизации косметических средств: теней, румян, туши и пр.
Домоводство
Распространено добавление вещества в огородные азотные удобрения. Используют, в качестве подкормки в вегетационный период (для роста и развития растений). В составе аммонийного карбоната для удобрений содержится 24% азота. Контактируя с воздухом, аммиак испаряется, вещество превращается в бикарбонат натрия.
Углекислый аммоний добавляют в вещества для чистки оружия и порошок для пожаротушения. Используется как самостоятельный реагент, так и в комплексе с натриевыми бикарбонатами, гидроксидами, гидрокарбонатами.
Воздействие на человеческий организм
Пищевой эмульгатор Е503 безопасен для живых существ. Техническая версия вещества – агрессивна, взрывоопасна. Возможно поражение тканей, вплоть до летального исхода.
Польза
Пищевую добавку Е503 не употребляют в чистом виде, только в продуктах промышленного производства. Пользы для человеческого организма нет, как и вреда. В процессе термической обработки, вещество разрушается, выделяются вредные газы и компоненты наружу, делая пищу полностью безопасной для употребления. В результате воздействия углекислого аммония в продуктах остается пористость, стабилизируется вкус, цвет.
Вред
Сравнительно с пищевой добавкой Е503, техническая угольноаммонийная соль опасна. Требует осторожности при использовании. Применяется в промышленности, поэтому сотрудникам предприятия важно знать меры предосторожности.
Из данных паспорта безопасности химической продукции от 9.03.2016 г. технический аммиак внесен в Регистр Росстандарта информационно-аналитическим центром «Безопасность веществ и материалов» ФГУП «ВНИИ СМТ».
Опасность для человека и живых существ:
- раздражает дыхательные пути (пары);
- вызывает химические ожоги, попадая в органы зрения, на кожный покров;
- при проглатывании разъедает пищеварительную систему.
Избегать утечки карбоната аммония в т.ч. отходов в водоемы. Чрезвычайная опасность для водных существ.
Симптомы поражения:
| Тип | Симптомы |
| Отравление при вдохе паров | Низкая концентрация вещества:
Высокая:
Критический уровень;
|
| Поражение кожного покрова | Краснота, болезненность, в области пораженного участка. При отсутствии первой помощи химический ожог, пузыри |
| Проникновение в органы зрения | Острое раздражение, ожоги слизистой оболочки |
| Проглатывание, повлекшее отравление | Ожог слизистой рта, боль в голове, краснота лица, отечность языка\губ, тошнотный рефлекс, рвота, возможно с кровяными выделениями.
В тяжелых случаях летальный исход. |
Оказание первой помощи пострадавшему:
| Тип поражения | Что делать |
| Отравление, путем проникновения паров углекислого аммония в органы дыхания | Вывести на улицу, обеспечить покой, тепло, теплые ингаляции с 2-3 кристаллами лимонной кислоты\уксусом |
| Кожный контакт | До приезда скорой помощи тщательно промойте пораженный участок теплой проточной водой, делайте примочки из 5%-го раствора лимонной, уксусной или борной кислоты.
Госпитализация обязательна! |
| Глаза | Промывайте глаза при полном раскрытии, в течение 10 мин. под проточной водой. При острой боли закапайте новокаином.
Срочная госпитализация, осмотр врача |
| Ротовая полость | Обильное питье 1-2% лимонного, уксусного раствора. Столовый из расчета 2 ст. л\1 ст. жидкости.
Выпить глотками 100 мл растительного масла, показаться специалисту |
| Рвоту не вызывать! | |
Тип пищевой добавки
Карбонатная аммонийная соль (карбонат аммония) – это пищевой консервант, Е503. Пищевая добавка считается полностью безопасной. Отличима от технической версии сниженной концентрацией. Применяется, в качестве кислотного регулятора, дрожжей, разрыхлителя, эмульгатора (индексы Е500-599). Смешивает до однородности жидкости разных консистенций, например: масло и воду.
Под термическим влиянием становится полностью безопасной. Опасна только в исходном техническом состоянии (для промышленного применения, удобрений).
Класс опасности и токсичность
В связи с различным влиянием на организм и окружающую среду, карбонату аммония присвоено несколько классов опасности.
Общие сведения о воздействии на организм по ГОСТу- малоопасное вещество 4 класс.
| Токсичность | Класс опасности |
| При проглатывании | 4 |
| Способность к раздражению кожи, некрозу тканей | 1В |
| Повреждение органов зрения (от раздражения до полной\частичной потери зрительной функции) | 1 |
| Для водной среды | 1 |
| Хроническая токсичность для водного мира | 2 |
| Избирательная токсичность на системы организма, органы-мишени (однократное воздействие) | 3 |
Предотвращение вредного воздействия при чрезвычайных\аварийных ситуациях:
- переместить поврежденную цистерну в безопасное место;
- устранить людей в радиусе 100 м+;
- после химической разведки оградить пораженный участок здания;
- держаться наветренной стороны, избегая низин;
- устранить источники искр, огня, включая спички. Не курить! Не поджигать!
- Оказать первую помощь.
Порядок ликвидации аварийной протечки:
- Вызвать газоспасателей;
- Сообщать в СанЭпидемНадзор;
- Устранить протечку, соблюдая меры предосторожности. Не прикасаться к веществу голыми руками;
- Перекачать жидкость в подготовленную емкость без коррозийных признаков;
- Протекшее вещество оградить землей, посыпать инертным сырьем, собрать в металлическую без коррозийную тару.
- Создать водяные навесы по периметру газообразного облака.
Обеспечение пожаровзрывоопасности
Жидкий аммиачный раствор углекислого аммония не взрывоопасен, не горюч но, распадаясь, выделяет взрывоопасные концентрированные аммиачные пары. Выделяемый газ легко воспламеняется, загорается.
- самовоспламеняется в газообразном виде при 650;°C;
- в жидком растворе свыше 750°C.
Распространение пламени в кислороде 15-28 объемных аммиачных долей. Аммиак – продукт термической деструкции. Не вдыхать! Оказывает раздражающее и прижигающее действие на бронхиально-легочную систему.
Запрещенных средств для пожаротушения не выявлено. Можно использовать воду, пену, инертные газы. тушить с максимального расстояния для обеспечения безопасности. Тушить в огнеупорном костюме с самоспасателем, использовать дыхательные аппараты с избыточным давлением.
Хранение и упаковка
Упаковывают углекислый аммоний в полиэтиленовые мешки, весом от 25 кг. Жидкий раствор в металлических цистернах, герметично закрытых крышкой. Хранят в сухих складских помещениях при температуре 15-25 °C, вдали от солнечных лучей. Срок хранения – 365 дней с даты изготовления.
Транспортировка
Любым видом транспорта, кроме воздушного, соблюдая правила перевозки взрывоопасных грузов.
Где купить и сколько стоит
Приобрести карбонат аммония можно у завода изготовителя, официального дистрибьютора или через интернет. Они помогут определиться с количеством, организуют доставку, согласно правилам перевозки. Стоимость от 30 руб\кг. Возможна покупка оптом. Соответственно цена снизится, уточняйте у поставщика.
Пищевой карбонат аммония – это пищевая добавка E503, которая считается безопасной для человека. Технический карбонат аммония способен повлечь смерть при ингаляционном и пероральном поражении. На воздухе вещество воспламеняется. Соблюдайте меры предосторожности, работайте с веществом только в перчатках, не вдыхайте пары.
Читайте также:
















Оставить комментарий