Хлорид фосфора – это неорганическое соединение, фосфорная соль соляной кислоты. Существует два вида вещества, которые отличаются степенью окисления фосфора: +3 либо +5, им соответствуют хлорид III (трихлорид) и хлорид V (пентахлорид). Основная сфера потребления этих солей – химическая промышленность. Они используются для изготовления красок, пестицидов, в качестве реагента. В фармацевтике хлорид фосфора имеет важное значение, поскольку служит сырьём для разработки действующих компонентов лекарственных препаратов.
Содержание
Что такое хлорид фосфора, формула, виды
Хлорид фосфора представляет собой соединение фосфора и остатка хлорводородной кислоты, относится к классу солей. Атом фосфора может проявлять разную степень окисления. Окислительное число обозначает условный заряд элемента, который он приобретает после перемещения электронов. Оно может быть как положительным (при отдаче электронов), так и отрицательным (при принятии электронов). При взаимодействии с металлами и водородом фосфор находится в отрицательной степени окисления -3, с более сильными окислителями он показывает положительное окислительное число, т.к. отдаёт электроны. Поэтому с хлором может образовываться две разновидности соединений:
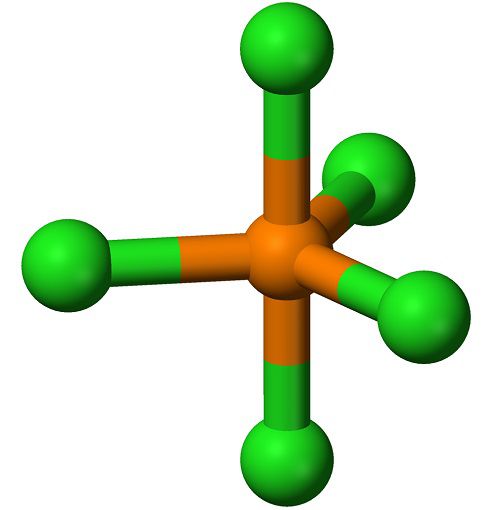
- хлорид фосфора (V), другие названия: пентахлорид фосфора, хлорангидрид фосфорной кислоты; фосфор находится в максимальной степени окисления +5, хлор забирает все его неспаренные электроны; химическая формула: PCl5;
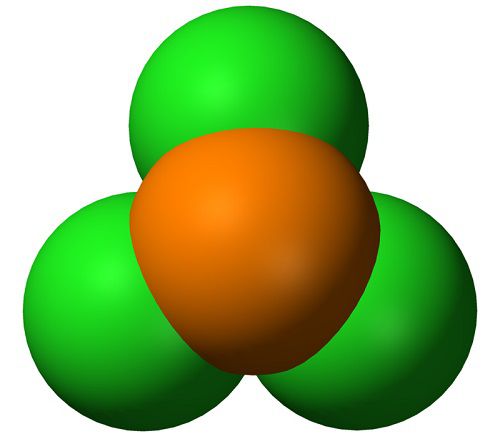
- хлорид фосфора (III) (трёххлористый фосфор либо трихлорид фосфора), фосфор имеет степень окисления +3, формула вещества PCl3.
Оба варианта солей были открыты британским химиком Гэмфри Дэви, который одновременно синтезировал и пентахлорид, выделившийся в виде кристаллов, и трихлорид, образовавшийся в виде жидкости. Они проявляют различные физико-химические свойства, что связано с разным набором атомов и состоянием их электронных полей.
Физические свойства, внешний вид
Хлорид фосфора (V) при нормальных условиях имеет вид порошка зеленовато-жёлтых или беловатых кристаллов без запаха, низкой плотности, рассыпчатых. Может существовать в жидком и газообразном состоянии, при этом пары очень тяжёлые, в 7,2 раз плотнее воздуха. Температура плавления – 160 °С. Переходит из твёрдого вещества в газообразное, минуя жидку фазу, при 159 °С. Термическое разложение происходит при температурном режиме, достигающем 300 °С. Вступает в реакцию с водой, растворяется в органических растворителях: бензол, хлоруглеродистые соединения, сероуглерод.
Хлорид фосфора (III) представляет собой жидкость, не имеющую цвета. Она источает резкий неприятный запах, обладает слезоточивыми свойствами. При высокой влажности дымится. Плавится при отрицательной температуре, порядка -93,6 °С, кипит при нагревании до 76,1 °С.
Реакции со хлоридом фосфора и химические свойства
Хлорангидрид фосфорной кислоты проявляет свойства, типичные для других солей. За счет мощного остатка соляной кислоты (Cl) и кислотных свойств фосфора активно вступает в реакции окисления, особенно окислительного хлорирования:
PCl5 + 2NO2 → PCl3↑+ NO2Cl↑
При этом образуется смесь газов: пары трихлорида фосфора и хлорида нитрозила. При взаимодействии с водой происходит неполный гидролиз – разложение вещества с образованием хлорокиси фосфора и соляной кислоты:
PCl5 + H2O → POCl3 + 2HCl
При подогревании гидролиз идёт до конца и образуется ортофосфорная кислота и хлороводород:
PCl5 + 4H2O → H3PO4 + 5HCl
Пентахлорид фосфора может вступать в реакцию с сильными кислотами, при этом формируются их хлорангидриды. Например, при реагировании с концентрированной серной кислотой продуктом реакции является монохлорангидрид серной кислоты, также выделяется фосфорилхлорид и хлороводород:
PCl5 + H2SO4 → ClSO3OH + POCl3 + HCl
Хлорид фосфора (V) может вступать в реакцию полимеризации, при этом образуется полимер фосфонилхлорид. Взаимодействие с хлоридом аммония идёт при нагревании:
PCl5 + NH4Cl → (PNCl2)n + 4HCl
Фосфонилхлорид является неорганической заменой каучука, обладает эластичностью, выдерживает нагревание до высоких температур, прозрачен. Его существенный недостаток – подверженность гидролизу и быстрое разложение.
Хлорангидрид фосфорной кислоты вступает в реакции хлорирования. Хлорирование заключается в перенесении хлора из вещества на субстрат. Хлорирование неорганических веществ приводит к образованию хлоридов:
PCl5 + 6LiF → LiPF6 + 5LiCl
Хлорирование органических соединений связано с отщеплением атома водорода и замещением его хлором, либо заменой гидроксильной группировки (-OH). При пониженном температурном режиме хлорид фосфора (V) реагирует с уксусной кислотой:
PCl5 + CH3COOH → СH3COCl + POCl3 + HCl
Пентахлорид фосфора – ценное сырьё для получения реактива Вильсмайера. Вступая в реакцию с диметилформамидом, он приводит к образованию хлорида диметилхлорметиленаммония:
PCl5 + C3H7NO → [(CH3)2NCHCl]Cl
Данный реактив необходим для модификаций ароматических соединений, введения в их структуру альдегидных группировок (-CHO). Хлорид фосфора (V) является кислотой Льюиса, т.е. он притягивает электронную пару, образуя продукт прямого присоединения молекул друг к другу.
Трихлорид фосфора же, напротив, является основанием Льюиса. Вещества такого типа легче отдают электронную пару акцепторам (кислотам), чем принимают сами, это доноры электронов, проявляющие восстановительные свойства.
Хлорид фосфора (III) – предшественник других фосфорсодержащих соединений, он легко переходит в пентахлорид, оксихлорид и тиофосфорилхлорид фосфора. Вещество легко реагирует со спиртами, аминами и фенолами. Для него характерны реакции замещения – взаимодействия, при которых одна функциональная группировка замещается другой (в данном случае – хлором).
Трихлорид фосфора разлагается при смешивании с водой, при этом образуется фосфористая кислота, реакция идёт интенсивно:
PCl3 + H2O → H3PO3 + 3HCl
При реагировании с фенолами происходит образование фосфатов и фосфитов – солей фосфорной кислоты. Так, при взаимодействии с фенолом и другими соединениями фенольного ряда трихлорид фосфора даёт трифенилфосфит:
PCl3 + C6H5OH → P(С6H5O)3 + 3HCl
Со спиртами реакция протекает по схожему принципу при щелочном значении водородного показателя (в присутствии третичного амина):
PCl3 + C2H5OH + С6H9N → P(C2H5O)3 + C6H10NCl
Если не вносить в реакционную смесь амин, продукты получаются иные: диэтилфосфат, а также хлорид и соляная кислота:
PCl3 + C2H5OH → С2H5POH + 2HCl + C2H5Cl
Трихлорид фосфора может вступать в реакции с аминами и давать промышленно значимые вещества. Его способность реагировать с азотосодержащими реактивами используется для получения аминофосфонатов при добавлении формальдегида:
PCl3 + CH2O + СH3-NH2 → CH2PO(OH)2NCH3 + HCl
В ходе реакции образуется фосфорный аналог метиламина (первичная аминокислота), который применяется для производства гербицидов, агентов, способствующих очищению воды от примесей.
Хлорид фосфора (III) реагирует с щелочами, в результате образуется две соли: монофторофосфат натрия и хлорид натрия.
PCl3 + NaOH → Na2HPO3 + 3NaCl + 2H2O
Получение и производство
Хлорид фосфора (V) в лабораторных условиях получают путём окисления трихлорида фосфора хлором в газообразном состоянии:
PCl3 + Cl2 → PCl5
В промышленном получении используется эта же реакция, но при этом процесс идёт в несколько стадий и со сложным оборудованием:
- В реактор загружают хлорбензол и четырёххлористый углерод. Реактор снабжён холодильником, барботёром и мешалкой, что необходимо не только для протекания взаимодействия, но и для его интенсификации.
- Внутрь запускают газообразный хлор, повышают температуру среды до 45 °С. Образуются хлорфосфозены (соединения, в которых между азотом и фосфором имеется двойная связь).
- В реакторе повышают давление, оставляя смесь на 6-7 часов. В это время идёт образование трихлорида фосфора из загруженных ранее реагентов, он сразу же взаимодействует с хлором, преобразуясь в пентахлорид. Когда анализ проб покажет содержание хлорида фосфора (III) не менее 1%, прекращают внесение хлора.
- Под большим напором внутрь подают азот, продувают им смесь.
- Полученный хлорид фосфора (V) фильтруют и отправляют на щадящую сушку.
Ежегодно производят около 10 тысяч тонн пентахлорида. Трихлорида выпускается порядка 1/3 миллиона тонн. Несмотря на это, процесс получения трихлорида фосфора сложен в технологическом отношении в связи с его высокой реакционной способностью и быстрым переходом в пентахлорид. Основа лабораторного и производственного получения – взаимодействие белого фосфора с газообразным хлором:
P4 + 6Cl2 → 4PCl3
В промышленности добычу вещества осложняет необходимость постоянно забирать из реакционной смеси продукт, чтобы предотвратить его преобразование в пентахлорид. На некоторых заводах организована особая система производства, которая заключается в использовании аппарата, разделяющего реагенты. В нём есть отдельный сосуд, в который подают фосфор и труба для слива хлорида фосфора (III).
Промышленное производство трихлорида строго контролируется законодательством, поскольку соединение может быть использовано для производства химического оружия: иприта – боевого отравляющего вещества.
Воздействие на организм
Хлориды фосфора являются опасными ядами и крайне отрицательно воздействуют на здоровье человека. Трихлорид фосфора – удушливый газ, вызывающий обильное слезоотделение и раздражение слизистых оболочек. Пентахлорид – сильный неорганический яд, порошок при попадании на кожу вызывает глубокие химические ожоги за счёт мощных окислительных свойств.
При вдыхании паров хлоридов возникает рефлекторное сокращения гладкой дыхательной мускулатуры, появляется кашель с большим количеством мокроты, бронхоспазм, отёк лёгких. Случайное проглатывание приводит к отравлению, которое сопровождается рвотой, диареей, сильными режущими болями живота. Может наблюдаться поражение сердечно-сосудистой системы. При этом снижается частота сердечных сокращений, резко возрастает и падает артериальное давление. Возможно поражение центральной нервной системы, возникают судороги, параличи, кома.
Применение
Основная сфера применения хлоридов фосфора – химическая промышленность. Они используются для получения фосфорорганических соединений, необходимых для синтеза удобрений, пестицидов, гербицидов, лекарств. Эти соединения – незаменимые предшественники различных пластификаторов, масляных добавок. Хлориды применяются для получения углеводородов в органическом синтезе.
Применение хлоридов фосфора в химической промышленности
Хлорангидрид фосфорной кислоты – мощный хлорирующий агент. Он применяется в качестве осушающего вещества, т.к. проявляет дегидратирующие свойства. Хлорид фосфора (V) может быть использован для преобразования лекарственных средств. Некоторые синтетические препараты содержат его производные или технология их получения подразумевает применение пентахлорида для создания необходимой среды.
Назначение хлорида фосфора (III) более широкое, что связано с его большей реактивной способностью. Трихлорид применяется:
- при изготовлении лакокрасочных материалов;
- для производства реакционных смесей;
- как сырьё и реактив для реакций органического синтеза;
- для придания нужных свойств пластификаторам;
- в производстве антипиренов.
Поскольку трихлорид фосфора ядовит, на его основе создают средства, уничтожающие сорные растения (гербициды), препараты для избавления от возбудителей опасных заболеваний растений (пестициды), а также продукты для борьбы с насекомыми – инсектициды. Один из таких – диазинон, опасное фосфорсодержащее средство, использующееся как для борьбы с домашними насекомыми (тараканы, клопы, моль), так и для уничтожения вредителей сельского хозяйства: тля, муравьи, жуки.
Где купить и сколько стоит
Приобрести хлорид фосфора может только юридическое лицо с официальным разрешением, поскольку оборот его ограничен законодательно. Трёххлористый фосфор продают заводы-производители от 135 рублей за 1 кг. Пентахлорид продаётся не только оптом, но и в розницу в магазинах, специализирующихся на химических реактивах. Стоимость существенно отличается. Цена 1 кг вещества порядка 5500 рублей, в то время как 100 грамм можно купить за 800 рублей. Оптовая стоимость составляет около 120 руб/кг.
Токсичность, меры предосторожности
Хлорид фосфора – это крайне токсичное соединение. Оба вида относятся ко 2 классу опасности – высокоопасные вещества. 600 промилле (либо в концентрации 140 мг\м3) трихлорида фосфора – летальная доза, убивающая человека за несколько минут. Симптомы отравления при вдыхании могут проявиться не сразу, но действие яда на организм комплексное, т.е. поражаются сразу несколько систем органов. Пентахлорид приводит к серьёзным ожогам кожи и слизистых оболочек, провоцирует некроз и отмирание тканей, при попадании внутрь – расплавление органов. Предельно допустимая концентрация хлоридов фосфора в воздухе – 0,2 мг/м3.
Меры предосторожности заключаются в крайне аккуратном обращении с хлоридами фосфора. Необходимо надевать защитную одежду, покрывающую всё тело, а также носить респиратор, в котором регулярно менять фильтр. При предположительном отравлении необходимо немедленно обратиться к врачу. На производстве нужно соблюдать все требования техники безопасности.
Заключение
Хлорид фосфора – это неорганическая фосфорная соль соляной кислоты. В зависимости от степени окисления фосфора возможно существование двух разновидностей: пентахлорид и трихлорид. Они отличаются физико-химическими свойствами. Пентахлорид более стабилен, в то время как трёххлористый фосфор – более активен за счёт свободной электронной пары. Он легко преобразуется в другие фосфорсодержащие соединения, поэтому важен для органического синтеза и многих других реакций. Хлориды фосфора крайне опасны и смертельны для человека, других животных и даже бактерий. За счёт этого они применяются для изготовления пестицидов, инсектицидов и гербицидов. Кроме того, фосфорные соли соляной кислоты применяются для получения пластификаторов, красок, лекарственных препаратов.
Читайте также:














Оставить комментарий